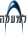מבנה ומנגנון הפעולה של הדפנסינים
דפנסינים הם משפחת פפטידים בעלי טווח רחב של פעילות אנטי-חיידקית, שמקורם בניטרופילים (α-defensins) או בתאי אפיתל
(β-defensins). מולקולות אלפא דפנסינים נמצאות בגרגירים האזורופיליים בניטרופילים, שם הן מהוות עד 50% מתכולת האברון, או
כ-5%-7% מכלל החלבון בתא הניטרופילי. כן נמצאים אלפא דפנסינים במאקרופגים, בכוכים של רירית המעי, ובעיקר בתאי Paneth המגורגרים במעי
הדק של רוב היונקים. ביתא דפנסינים נמצאים בניטרופילים של בקר, בליקוציטים של עופות, ובפלסמת הדם באדם, ולאחרונה דווח על הימצאותם
גם בתאי עור ובעין [2]. ארבעה סוגי דפנסינים נוצרים על-ידי ניטרופילים באדם ושלושה מהם (HNP1, HNP2 ו-HNP3) השונים אחד ממשנהו
בחומצה אמינית אחת, וביחד מהווים 99% מכלל הדפנסינים המופרשים על-ידי הניטרופיל. HNP4 זהה רק ב-32% מרצף חומצות אמיניות של הפפטידים
הניטרופיליים הקודמים, ועיקר פעילותו היא בעיכוב ההורמון הקורטיקוטרופי ACTH על-ידי קישור לקולטן של הורמון זה [3].דפנסינים הם פפטידים קטיוניים המורכבים מ-29 עד 35 חומצות אמיניות שמשקלם המולקולתי הוא 3.5 ק"ד בקירוב. הם עתירי ארגינין ומכאן מטענם החשמלי החיובי, והם ייחודיים בהכילם 6 שיירים של ציסטאין היוצרים שלושה קשרי -S-S- דיסולפידיים, תוך-מולקולתיים. דפנסינים מיוצר במקור כפפטיד קודמן המורכב מ-94 חומצות אמיניות בשלב הרשת האנדופלסמית, הידוע כ-prepropeptide והקצה האמיני שלו signal) (peptide טעון שלילית, כנראה כדי לנטרל את המטען החיובי של חלק המולקולה הסמוך לקצה הקרבוקסי, ולמנוע נזק לתא הפונדקאי עצמו. ביקוע אזור הקצה האמיני יוצר פפטיד-ביניים (prodefensin) המכיל 75 חומצות אמיניות ההופך בלשד העצם לתוצר ביניים בעל 56 חומצות אמיניות באמצעות ביקוע פרוטיאוליטי ליד שייר חומצה אספרטית, ומכאן המעבר למולקולת דפנסינים הסופית בתאים ניטרופיליים בדם ההיקפי [4]. המאמץ המרוכז להבין את מנגנון הבקיעה של ה-pro-defensin והסבתו לפפטיד פעיל, הביא לאחרונה לתיאורו של אנזים פרוטאוליטי-מכיל-יון-מתכת, matrilysin, הממוקם בתאי Paneth במעי ביחד עם מולקולת הקודמן של האלפא דפנסינים [5]. מסתבר, שלצורך שיפעולה של מולקולת דפנסין במעי, המכונה גם cryptdin משום מיקומה בכוכי המעי, מבקע ה-matrilysin את הקשר שבין שיירי ליוצין וארגינין, ואכן הדפנסין בהרכבו הסופי מכיל ליוצין בעמדת הקצה האמיני. עכברים טרנסגניים (MAT-/-) החסרים את האנזים matrilysin אינם מראים פעילות אלפא-דפנסינים, והפעילות האנטי מיקרובית של המעי נמוכה בהם: עכברים אלה היו פחות מסוגלים להשמיד חיידקי E. coli במעי, והייתה בהם תמותה רבה יותר אחרי הדבקה פומית בחיידקי Salmonella typhimurium, מה שממחיש את חשיבות ה-matrilysin בשיפעול הדפנסינים.
שיבוט הגן של שני סוגי הדפנסינים, אלפא וביתא, לאזור זהה בכרומוסום 8p23.1-p23.2, והעובדה שגם חלבונים אלה בעכבר נסרקו לאותו אזור בכרומוסום 8 מצביעה על גן-קדמון אבולוציוני משותף, ונראה אמנם שמנגנון פעולתם זהה. דפנסינים חודרים לתוך הקרומים של חיידקים גראם-חיוביים או שליליים, וכן לקרומי פטריות ונגיפים, ויוצרים בהם תעלות יונים הרגישות למתח חשמלי, ובכך מביאים להגברת החדירות והתמותה של מיקרואורגניזמים אלה [6]. נמצא, שמולקולות דפנסינים יוצרות דימרים ואפילו טטרמרים ופולימרים טעונים חיובית. אלה נקשרים למולקולות ליפופוליסוכרים (LPS) הטעונות מטען שלילי בקרומים החיצוניים ואף הפנימיים של דופן החיידק, לפני החדירה ויצירת נקבים (pores) בדופן [7] (תמונה 1). בחינת החדירות הקרומית על-ידי תבחין קליטת הצבע טריפאן-כחול מראה, שכבר לאחר 60 דקות מתחילת הדגרת חיידקים עם אלפא דפנסינים ונקלט בהם צבע-הבוחן המעיד על נזק תאי בלתי-הפיך [8].

תמונה 1: מנגנון הפגיעה בחיידקים על-ידי פפטיד קטיוני, כמו דפנסין. הפפטיד הטעון חיובית (1) נקשר אלקטרוסטטית לשכבה הפוספוליפידית הטעונה שלילית על שטח פני החיידק (2). בהמשך, משתרבב הפפטיד לתוך ממברנת החיידק (3) ויוצר תעלות דרכן דולפות מן הציטופלסמה של החיידק מולקולות חיוניות, וממילא נגרם מות החיידק.
אלפא-דפנסינים ממקור ניטרופילים
Welling וחב' [9] בחרו את השימוש הפוטנציאלי ב-HNP-1 למניעת הדבקות חיידקים במערך ניסויי, בו הודבקו עכברים תוך-ציפקית ב-Klebsiella
pneumoniae. הזרקה מילעורית של 1 מיקרג' HNP-1 הביאה להפחתה ניכרת במספר החיידקים בחלל הצפק 24 שעות לאחר ההדבקה היזומה
והטיפול בדפנסינים. הפעילות האנטי-בקטרית של HNP-1 היתה כרוכה בהסננת מאקרופגים, גראנולוציטים ולימפוציטים בחלל הצפק. בדומה, הדבקה
ניסויית ממוקדת של עכברים ב-K. pneumoniae או סטפילוקוק זהוב לתוך שריר הירך, הושפעה אף היא על-ידי הזרקה מקומית של HNP-1
באופן שהפחית משמעותית את כמות החיידקים ששרדו, כאשר סומן HNP-1 על-ידי האיזוטופ Tc99m, הודגם, שדפנסין זה התרכז זמן קצר לאחר
הזרקתו באזורים הנגועים בחיידקים. עובדה זו פותחת אפשרות לשימוש בדפנסין רדיואקטיבי למיקום ואיתור הדבקות מקומיות וסמויות בחיידקים.
מנגנון הפעולה בו מביאה הזרקת כמות מיזערית של דפנסינים להשפעה משמעותית בדיכוי הדבקה בחיידקים, אינו מתבצע כנראה בפעולה ישירה של
הדפנסינים על החיידקים, אלא בהשפעה משנית של הדפנסינים בהשראת מהלך של גירוי והכוונה (chemotaxis) של ליקוציטים למיניהם לאזור הנגוע
בחיידקים.Ashitani וחב' [10], מדדו רמות אלפא דפנסינים בתפליט צידרי (pleural effusion) במצבים פתולוגיים שונים של הריאה, במטרה לבחון את התאמתם האפשרית כסמן איבחוני. מדידות אלה הדגימו באופן משכנע רמות מוגברות במיוחד של דפנסינים במצבי מימגלת (empyema) כאשר הרמה הממוצעת שנמדדה היתה כ-13,300 מיקרג'/ל' בהשוואה ל-160 מיקרג/ל' שנקבעה בנוזל הדיית (transudate) בנבדקי בקרה. רמת הדפנסינים שנמדדה במצב של מימגלת הייתה גבוהה באופן בולט אף מהרמה שנמדדה בנוזל צידרי של חולים עם דלקת ריאות, שחפת, שאת הריאה ואוורת בית-החזה (pneumothorax) - (ריכוזים של 200, 800, 200 ו-200 מיקרג'/ל', בהתאמה). עם זאת יצויין, שכמות הליקוציטים, ובתוכם מקטע הניטרופילים גבוה פי-10 ומעלה בתפליט הצידרי במימגלת, בהשוואה למספרם במצבים פתולוגיים אחרים. כמו כן, רמת שני הציטוקינים IL-8 ו-G-CFF (המשרן של יצירת מושבות גראנולוציטים) בתפליט המתנקז במימגלת, גבוהה אף היא בהשוואה לרמתם במצבים פתולוגיים אחרים בריאות, מה שמביא להסננה מרובה של ניטרופילים בחלל הריאתי, וממילא להפרשת דפנסינים מרובה.
Mizukawa וחב' [11], מדדו רמת HNP-1 בדגימות רוק של מטופלים באירועים דלקתיים בחלל-הפה, בהשוואה לנבדקי בקרה. נמצא, שבעוד שרמת הדפנסינים ברוק של נבדקים בריאים היא 0.8 מיקרג'/מ"ל, ממוצע רמת דפנסינים ברוק של מטופלי דלקת פומית נקבע כ-14.7 מיקרג'/מ"ל. באותם חולים שטיפול הביא לריפוי ולהיעלמות הדלקת, ירדה מיידית רמת הדפנסינים ברוק לרמה התקינה של 0.8 מיקרג'/מ"ל. העלייה והירידה ברמת דפנסינים ברוק היתה מקבילה לתנודות דומות ברמת C-reactive protein בדם, שהוא מדד מקובל למצב דלקתי בהיותו acute phase protein.
הגברה משמעותית ברמת הדפנסינים הניטרופיליים (HNP1-HNP3) בפלסמה של פרטים במהלך הדבקה חיידקית, נמצאה בחולים עם אלח-דם (ממוצא הריכוז 29,800 מיקרג'/ל'), לעומת חולים בדלקת עוצבה חיידקית (660 מיקרג'/ל'), כאשר הריכוזים התקינים שנמדדו לאחר טיפול והחלמה באותם פרטים היו פחות מ-231 מיקרג'/ל' [12]. גם Ihi וחב' [13], שהשתמשו בתבחין-RIA רגיש, מצאו עליות בולטות ברמת הדפנסינים HNPI-HNP3 בחולים במצבי דלקת, כאשר רמתם הממוצעת בפלסמה של קבוצת בקרה היא 255 מיקרג'/ל'.
Heine וחב' [14] בדקו את ההשערה, שרמת הדפנסינים מקבוצת HNP1-3 מוגברת במי-השפיר של יולדות טרם-זמנן עם הדבקה תוך-רחמית תת-קלינית (IUI). נוזלי שפיר נדגמו מ-203 נשים הרות עם מאפיינים קליניים שונים, ורמות הדפנסינים נמדדו בשיטת ELISA. נמצא, שרמות הדפנסינים היו גבוהות פי 24-4 באלה עם IUI בהשוואה ליולדות טרם-זמנן או כאל ה שהשלימו תקופת הריון מלאה, ללא עדות להדבקות תוך-רחמיות. מידת ההגברה ברמת דפנסינים במי-השפיר עמדה ביחס ישיר לצמיחת חיידקים בתרבית, והגברה מרובה במיוחד של דפנסינים נמצאה בנבדקות עם חומרה מובהקת של ממצאים היסטולוגיים של דלקת קרומי השיליה (chorioamnionitis). בעוד שרמת הדפנסינים הממוצעת במי-שפיר של נשים בסוף הריונן בקבוצת הבקרה היא 202 מיקרוג'/ל', ביולדות טרם-זמנן מאובחנות עם IUI וצמיחת חיידקים בתרבית, רמת דפנסינים ממוצעת הגיעה לכ-15,800 מיקרג'/ל', ואילו במאובחנות IUI בהן תרבית החיידקים נמצאה שלילית נקבעה רמת דפנסינים ממוצעת כדי 750 מיקרג'/ל'. כיוון שרמות דפנסינים ברמה מעל 2,500 מיקרג'/ל' נמצאו ב-88% מכלל הנבדקות, עם ראיות להדבקה חיידקית תוך-רחמית, מבוצעים כיום ניסויים למדידת רמות דפנסינים בדגימות הנלקחות מהפרשות או רקמות מצוואר הרחם או מהלדן, בגישה פחות חודרנית. על-פי תוצאות רמתו במי-השפיר, דפנסינים יכול לשמש כמדד רגיש ל-IUI תת-קליני.
בתהליכי הדבקות חיידקיות ודלקת, הניטרופילים הם מראשוני הליקוציטים העוברים הסננה ברקמות ההיקפיות וברירית. בדומה, תאים חבויים ברירית המעי כמו תאי Paneth, הם תאים המקדימים לפגוש אנטיגנים זרים במערכת העיכול. לכן, קיימת סבירות שדפנסינים המופרשים מניטרופילים, ו-cryptdins שהם הדפנסינים המופרשים מתאי Paneth במגע עם החיידקים הפולשים, ישפיעו על לימפוציטים הנוכחים באזור חדירת האנטיגן הזר, וישרו תגובה חיסונית "סתגלנית" (adaptive). ניסויים להבנת מנגנוני ההשראה של חסינות נרכשת בפונדקאי על-ידי דפנסינים מניטרופילים (HNP), נעשוש לאחרונה על-ידי Lillard וחב' [15]. כאשר הזריקו לעכברים תוך-ציפקית HNP יחד עם האנטיגן Keyhole limpet hemocyanin (KLH), הוגברו משמעותית תגובות החיסון ההיקפי לאנטיגן החלבוני בהשוואה לעכברים בהם הוחדר KLH בלבד. כמו כן, הודגמה השפעת HNP על החסינות הנרכשת ברירית דרכי-הנשימה; כאשר הוחדר HNP ביחד עם האנטיגן החלבוני ovalbumin לאפם של עכברים, נצפתה בנסיוב יצירה מוגברת של נוגדני IgG סגוליים ל-ovalbumin. בדומה, בעכברים שחוסנו בחלבון האחרון בתוספת לדפנסין HNP, הדגימו תאי T מסוג CD4+ תגובה שיגשוגית סגולית ל-ovalbumin שהיתה חזקה יותר, וכן נקבעה יצירה מוגברת של גאמא-אינטרפרון, והציטוקינים IL-6, IL-5, ו-IL-10. במדידות in vitro באותם עכברים, הגביר HNP תגובה שיגשוגית של תאי T משופעלים על-ידי CD3 וכן את תגובת תאי B משופעלים על-ידי ליפופוליסוכר (LPS) ותאי T ו-B אלה היו ממקור טחול או Peyer's patch. ניסויים אלה מדגימים שדפנסינים מגבירים תגובה מערכתית של נוגדני IgG באמצעות ציטוקינים ממקור לימפוציטים, כגון CD4 Th1 ו-CD4 Th2. נראה שדפנסינים יכולים לתווך ולעודד יחסי-גומלין בין לימפוציטים מסוג T ו-B, ולקשר בין חיסון מלידה וחיסון נרכש.
ביתא-דפנסינים ממקור תאי אפיתל
תאי אפיתל מפרישים דפנסינים כחלק ממנגנון ההגנה המיידי שלהם (תמונה 2). לאחרונה אופיינו שני דפנסינים מקבוצת ביתא באדם HBD-1 ו-HBD-2.
HBD-1 מתבטא באופן מובנה (constitutive) באבוביות הכיליה, באיברי הרבייה ובמידה פחותה בלבלב ובתאי הפיתל בעור. בשיטות של RT-PCR וכן
באמצעות היברידיזציה in situ, הוכיחו את מיקומו של HBD-1 בקרטינוציטים בעור [16]. לעומתו, מושרה HBD-2 בעור ובתאי אפיתל שונים
בתהליכים דלקתיים. מסתבר שבריכוזים שמתחת ל-1 מיקרומול/ל', מסוגלים שני דפנסינים אלה לגרות ולהשרות תגובה בשני סוגי תאים של מערכת
החיסון: דנדריטים לא-בשלים ותאי זיכרון-T. הדנדריטים המתפתחים בלשד העצם, ומתיישבים באופן זמני באיברים לא-לימפואידיים, וחשיבותם
כתאים מציגי-אנטיגן ללימפוציטים TH [1]. נמצא, שדנדריטים ותאי-זיכרון-T מכילים על פניהם חלבון המכונה CCR6 המשמש קולטן לציטוקין
הפועל באופן סגולי על דנדריטים, המוכר כ-MIP-3 והידוע גם כ-LARC (Liver and Activation Regulated Chemokine). נמצא, ששני הדפנסינים
האמורים מתחרים עם LARC על הקישור לקולטן CCR6, ובהתאם הם מסוגלים להשרות גירוי לשיפעולם של תאי-זיכרון T ותאים דנדריטיים. לכן,
תאי-אפיתל נפגעים בעת הדבקה חיידקית מקומית, HBD-1 ו-HBD-2 ישתחררו ויביאו לגיוסם של תאי-החיסון האמורים, ובכך יסייעו להופעת חיסון
פעיל (adaptive). היכולת של מספר דפנסינים לשמש כמולקולות מאותתות המשפעלות תאים של המערכת החיסונית, יכולה להסביר לעתים את פעילותם
הביולוגית אף בריכוזים נמוכים ביותר, שאין בהם כדי לגרום נזק כימי ישיר לחיידקים [17].
תמונה 2: דגם של תגובת אפיתל הרירית לאתגר חיידקי: חיידק הבא במגע עם שכבת האפיתל, מגרה פעילויות אנטי-חיידקיות מקומיות, כגון הפעלת החלבון ליזוזים, הפרשת יונים רעלניים לחיידק כ-NO2 ו-H+, ושחרור פפטידים, כמו דפנסין, שכולם אחראים למות החיידק. בהמשך, נוצרות התגובות ארוכות-הטווח של הפונדקאי, כגון תהליך דלקת, והחיסון הנרכש. על פי [26].
Valore וחב' [18], בחנו בשיטה של Northern blot הימצאות HBD-1 ברקמות שונות. הריכוזים הגבוהים ביותר של m-RNA של דפנסינים התגלו בשיטת היברידיזציה in-situ בכיליה, בעיקר שכבת האפיתל של לולאות Henle באבוביות הרחיקניות ובצינורות האיסוף בכיליה. ריכוזים גבוהים במידה דומה של דפנסינים באיברי הרבייה הנשיים, נמצאים באפיתל הלדן, ברחם ובצוואר הרחם וכן בצינורות ה-Fallopian. פפטידי דפנסינים מסוג HBD-1 שהכילו בעיקר 40-36 חומצות אמיניות, היו בעלי פעילות אנטי-חיידקית בתחום ה-pH החומצי המקובל בשתן, ובדומה לדפנסינים מקבוצת HNP, גם הם איבדו פעילותם בריכוז מלחים גבוה, שאינו מצוי בדרך כלל בשתן. מציאות ריכוז גבוה של HBD-1 במערכות כילייתיות ואיברי הרבייה הנשיים, יכולה לתרום להגנה מקומית בפני חיידקים.
Haynes וחב' [19], דווחו לראשונה על מציאות דפנסינים בעין, ומצביעים על החשיבות של פפטיד הגנתי זמין זה בדלקות עין מקומיות, ובמניעת דלקת הקרנית, בעיקר במצבים של כשל בהפרשת דמעות ויובש פני העין, הרכבת עדשות מגע ומצבי חירום כניתוחי עין. תוך שימוש בנוגדנים חד-שבטיים וצביעות היסטולוגיות, הוכחה נוכחותם של הדפנסינים, HNP1-HNP3 בלחמית במצב דלקתי, וכן בצינוריות בלוטת הדמעות ובנוזל דמעות תקין. שיטות RT-PCR הדגימו m-RNA של HBD-1 בקרנית, בלחמית ובבלוטת הדמעות. בדומה נמצא m-RNA של HBD-2 בקרנית ובלחמית, אך לא בבלוטת הדמעות. חוקרים אלה מעלים את האפשרות של שימוש במולקולות דפנסינים רה-קומביננטיות לטיפול במצבי דלקת, שכן הן לכאורה בעלות טווח רחב יותר של פעילות אנטי-חיידקית בהשוואה לחלופה של תכשירים אנטיביוטיים.
באחת הסוגיות המסקרנות קיימת התייחסות לפעילות של דפנסינים ברירית הריאות של חולים בלייפת כיסתית (CF), המאופיינת במצבי דלקת נשנית או כרונית. Singh וחב' [20] מצאו ביטוי של m-RNA של שני הב"ד, HBD-1 ו-HBD-2 באפיתל הריאה וכן באפיתל הבלוטות התת-ריריות, בחולי CF ובאנשים בריאים. שני הפפטידים נמצאו בנוזל BAL בריכוזים נמוכים של מתחת ל-10 מיקרג'/ל', ובשניהם הובחנה רגישות דומה לעליית ריכוז מלח בישול: בריכוז NaCl של 150 מילימולר חלה ירידה של 80% ביכולת של HBD-1 ו-HBD-2 להרוג חיידקי E. coli. יחד-עם-זאת, נמצאו הבדלים מהותיים בהתנהגות שני דפנסינים אלה במדדים אחרים: הציטוקין הקדם-דלקתי β1 ו-IL הביא בתרבית ראשונית של תאי-אפיתל מדרכי-האוויר לביטוי m-RNA של HBD-2 להתהוות דפנסינים זה, אך לא לביטוי של HBD-1. זאת ועוד, HBD-1 נמצא בנוזל BAL של מתנדבים בריאים, מחולי CF ומחולים במחלות ריאה דלקתיות. לעומתו, HBD-2 נתגלה בנוזל BAL מחולי CF או כאלה עם מחלות ריאה דלקתיות, אך לא בנוזל מריאות בקרה בריאות. נתונים אלה רומזים, שביטוי הדפנסינים HBD-2 בריאות מושרה על-ידי תהליך דלקתי, כאשר HBD-1 משמש להגנה אף בהעדר מצב דלקתי. האם אמנם העלייה הידועה בריכוז המלח ברקמת הריאה של חולי CF קשורה באיבוד חלקי של פעילות דפנסינים, וממילא בהחלשת ההגנה מהדבקה חיידקית, לכך יידרשו מחקרים נוספים [21].
פעילויות ביולוגיות נוספות של דפנסינים: העניין הרב שגבר בעשור האחרון סביב הדפנסינים, הביא למספר מסקנות שאינן קשורות דווקא לפעילות ההגנתית האנטי-חיידקית הישירה של פפטידים אלה. Befus וחב' [22] מדווחים שדפנסינים ממקור אדם (HNP1, HNP4) וכן דפנסינים ממקור ניטרופילים של חולדה, חזיר-ים וארנבת, מדגימים פעילות שיחרור היסטאמין מתאי פיטום (mast cell). כמו כן מסוגלים דפנסינים אלה להשרות דה-גראנולציה בתאי פיטום, אך באופן השונה מזה המושרה בתאים אלה על-ידי אנטיגן או אלרגן בתלות ב-IgE. תאי-פיטום שהודגרו עם דפנסינים, הגיבו בשיפעול חלבון G במקטע הממברנתי, והתגובה היתה דומה לזו שהושגה על-ידי substance P, ונראה שדפנסינים מאפשר מסלול חשוב של התקשרות בין ניטרופילים ותאי-פיטום כהגנה מפני אנטיגן חיידקי או בעת תגובה דלקתית חדה. מנגד, נמצא, שדפנסינים ממקור ניטרופילים, HNP1, מעכב את השיפעול של המסלול הקלסי של המשלים על-ידי עיכוב הפעילות ההמוליטית של Clq. נמצא, ש-HNP1 יכול להתקשר באופן חלקי גם ל-Cl, ועל כל פנים קישור זה של הדפנסינים למרכיבי המשלים, עלול להביא להמעטת פעולת המשלים, והתגובה הדלקתית הקשורה עם פעולת הניטרופילים עצמם [23]. ואמנם, גם בהיבט אחר נמצא, שדפנסינים עלולים לפגוע לכאורה בפעילות ההגנתית המיוחסת לניטרופילים. Kaplan וחב' [8] הדגירו ניטרופילים עם HNP1 ומצאו, שנגרמה בתלות בריכוז הדפנסינים, הפרעה בייצור רדיקלים חופשיים של חמצן בניטרופילים המטופלים בדפנסינים, ונחלשה יכולתם הפאגוציטית להרוג חיידקים. כלומר, שחרור HNP על-ידי ניטרופילים הבאים במגע עם חיידק פולשן, אמור לסייע בפגיעה בחיידק, אך עלול גם להחליש (down regulation) פעילות אנטי-חיידקית אחרת של הניטרופיל.
היבט שלילי אחר שמייחסים לפעילות דפנסינים המשתחררים מניטרופילים דווח על-ידי Gorter וחב' [24]. נמצא, שדפנסינים (HNP1-HNP3) שבודדו מדגימות כיח של מטופלים עם מחלת ריאות כרונית (COPD), לא הרגו חיידקי Haemophilus influenzae המשתתפים בהדבקות נשנות של דרכי הריאה התחתונות בחולים אלה. לעומת זאת, דפנסינים אלה עודדו את הספיחה של חיידקי ההמופילוס לתאי-אפיתל ריאתיים באדם: הדגרת תאי אפיתל, חיידקי המופילוס ו-HNP1 הביאה לאחר 3 שעות להגברה פי-61 במידת הספיחה, ונראה שדפנסינים עלולים להגביר את הפתוגניות של חיידק זה בדרכי הריאה התחתונות.
השפעה פתולוגית מעניינת נוספת עולה ממחקרי Cines וחב' [25] על מעורבות דפנסינים (HNP1, HNP2) בתהליך טרשת העורקים. חוקרים אלה דיווחו בעבר שדפנסינים ממקור ניטרופילי נוכחים ברבדים טרשתיים ומסייעים בקישור Lp(a) לתאי האנדותל. כעת נמצא, שדפנסינים עודד את קישור Lp(a) לחומר החוץ-תאי של דופן כלי-הדם (ECM) פי-40 ובאופן בלתי-הפיך. דפנסינים יוצר מכלול רב-ערכי עם שני מרכיבי LP(a): apoprotein (a) ו-LDL. בנוסף, מגביר דפנסינים את קישורו של Lp(a) לחלבון פיברונקטין פי-30 בהשוואה לקישור הטבעי של שני מרכיבים אלה. השפעת דפנסינים בחיזוק הקשר בין ליפופרוטאין אתרוגני ו-ECM אנדותלי, יכולה להגביר את התהליך הטרשתי.
לסיכום, משפחת פפטידי ה-defensin ממקורות התאים השונים, ובעיקר הניטרופילים, עלתה בעשור האחרון למוקד העניין המחקרי והקליני. עדיין לא מובנות כל ההשפעות של תוצר מובהק זה של החיסון הטבעי (innate) על התגובה החיסונית הנרכשת [26]. במחקרים רבים הנמצאים בעיצומם, יוכח אם אמנם מוצדקות התקוות שתולים בדפנסינים בגישה טיפולית אנטי-חיידקית, בעידן בו גוברת והולכת העמידות הנרכשת של חיידקים לתכשירים אנטיביוטיים קיימים.
ביבליוגרפיה
- Fearon DT & Locksley RM., The intructive role of innate immunity in the acquired immune response. Science. 1996; 272: 50-4.
- Ashitani J. Mukae H. Nakazato MS & al., Elevated pleural fluid levels of defensins in patients with empyema. Chest. 1998; 113: 788-94.
- Wilde CG. Griffith JE. Marra MN & al., Purification and characterization of human neutrophil peptide 4, a novel member of the defensin family. J Biol Chem. 1989; 195: 1336-44.
- Nakazato M. Shiomi K. Date Y & al., Isolation and sequence determination of 6- and 8-kDa precursors of human netrophil peptides from bone marrow, plasma and peripheral blood neutrophils. Biochem Biophys Res Commun. 1995; 211: 1053-62.
- Wilson CL. Quellette AJ. Sarthell DP & al., Regulation of intestinal -defensin activation by the metalloproteinase Matrilysin in innate host defense. Science. 1999; 286: 113-7.
- Kagan BL. Selsted ME. Ganz T & al., Neutrophil antimicrobial peptides (defensins) form voltage-dependent ionic channels in planar lipid bilayer membranes. Proc Natl Acad Sci (USA). 1990; 87: 210-4.
- Hill CP. Yee J. Selsted ME & al., Crystal structure of defensin HNP-3, an ampiphilic dimer: mechanisms of membrane permeablization. Science. 1991; 251: 1481-5.
- Kaplan SS. Heine RP & Simmons RL., Defensins impair phagocytic killing by neutrophils in biomaterial-related infection. Infect Immun. 1999; 67: 1640-5.
- Welling MM. Hiemstra PS. Van den Barselaar MT & al., Antibacterial activity of human neutrophil defensins in experimental infections in mice is accompanied by increased leukocyte accumulation. J Clin Inves. 1998; 102: 1583-90.
- Ashitani J. Mukae H. Nakazato M & al., Elevated fluid levels of defensins in patients with empyema. Chest, 1998; 113: 788-94.
- Mizukawa N. Sugiyama K. Ueno T & al., Levels of human defensin-1, an antimicrobial peptide, in saliva of patients with oral inflammation. Oral Surg Oral Med Oral Pathol. 1999; 87: 539-43.
- Panyutich AV, Panyutich EA, Krapivin VA & al., Plasma defensin concentrations are elevated in patients with septicemia or bacterial meningitis. J Lab Clin Med, 1993; 122: 202-7.
- Ihi T. Nakazato M. Mukae H & al., Elevated concentrations of human neutrophil peptides in plasma, blood and body fluids from patients with infections. Clin Infec Dis. 1997; 25: 1134-40.
- Heine RP. Wiesenfeld H. Mortimer L & al., Amniotic fluid defensins: potential markers of subclinical intrauterine infection. Clin infec Dis. 1998; 27: 513-8.
- Lillard JW. Boyaka PN, Chertov Q & al., Mechanisms for induction of acquired host immunity by neutrophil peptid defensins. Proc Natl Acad Sci (USA). 1999; 96: 651-6.
- Fulton C. Anderson GM. Zasloff M & al., Expression of natural peptide antibiotics in human skin. Lancet, 1997; 350: 1750-1.
- Yang D. Chertov Q. Bykovskaia SN & al., β-defensins: linking innate and adaptive immunity through dendritic and T cell CCR6. Science. 1999; 286: 525-8.
- Valore EV. Park CH. Quayle AJ & al., Human β-defensin-1: an antimicrobial peptide of urogenital tissues. J Clin Invest. 1998; 101: 1633-42.
- Haynes RJ Tighe PJ & Dua HS. Innate defence of the eye by antimicrobial defensin peptides. Lancet, 1998; 352: 451-2.
- Singh PK. Jia HP. Wiles K & al., Production of β-defensins by human airway epithelia. Proc Natl Acad Sci (USA). 1998; 95: 14961-6.
- Goldman MJ. Anderson GM. Stolzenberg ED & al., Human β-defensin-1 is a salt sensitive antibiotic in lung that is inactivated in cystic fibrosis. Cell, 1998; 88: 553-60.
- Befus AD, Mowat C. Gilchrist M & al., Neutrophil defensins induce histamine secretion from mast cells: mechanisms of action. J. Immunol. 1999; 163: 974-53.
- van den Berg RH. Farber-Krol MC, van Watering S & al., Inhibition of activation of the classical pathway of complement by human neutrophil defensins. Blood, 1998; 92: 3898-903.
- Carter AD. Eijk PP. Van Watering S & al., Stimulation of adherence of Haemophilus influenzae to human lung epithelial cells by antimicrobial neutrophil defensins. J Infect Dis. 1998; 178.
- Bdeir K. Cane W. Canziani G & al., Defensin promotes the binding of lipoprotein(a) to vascular matrix. Blood, 1999; 94: 2007-19.
- Huttner KM & Bevins CL, Antimicrobial peptides as mediators of epithelial host defense. Pediatr Res. 1999; 45: 785-94.