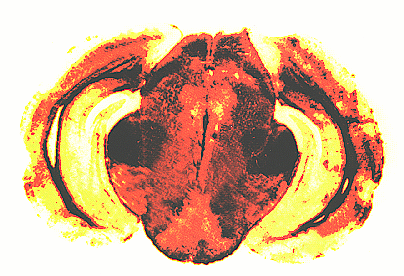
מיפוי חלבון הסקרפי בחתך מוח של אוגר נגוע במחלה. על חתך המוח הונחו נוגדנים כנגד חלבון הסקרפי שהתקשרו בכל מקון בו מצוי החלבון. באזורים הכהים מצוי החלבון הפגום בצפיפות גדולה.
במערכות ביולוגיות המידע הגנטי המורש מדור לדור מוצפן בדרך כלל במולקולות מיוחדות - חומצות הגרעין. לכל יצור-חי - נגיף, חיידק, צמח, בעל- חיים ואדם - חומצות גרעין משלו, שבהן רשומות ושמורות ההוראות הנחוצות לקיומו. חומר תורשתי זה הוא הבסיס המולקולרי לאבולוציה הדרווינית. לא ייפלא, אפוא, שגילויים של גורמי מחלה, המתרבים לכאורה ללא מעורבותן של חומצות גרעין, העלה תמיהה רבה בקרב הקהילה המדעית. נביא כאן את סיפורם המרתק של הפריונים (prions) - חלקיקים ביולוגים מוזרים, הגורמים מחלות קטלניות בבעלי חיים ובאדם, שככל הנראה אינם כוללים חומצות גרעין. טבעם המיוחד של הפריונים מסביר את היותם קשורים במחלות תורשתיות ובמחלות מידבקות כאחד.
מה לקניבלים מגיניאה החדשה ולכבשים הנגועות בגרד?
מחלת גרד הכבשים - סקרפי (scrapie), בה החיות החולות מתגרדות באופן נמרץ עד כדי איבוד הפרווה, היא מחלה קטלנית המתבטאת בהרס של תאי עצב במוח ובהופעת רקמת מוח ספוגית. כבר בשנות ה-40 היה ברור שמחלת הסקרפי של הכבשים מידבקת: הזרקת תמצית מוח של כבש נגוע לכבשים בריאים חולל - לאחר זמן דגירה ארוך מאוד - מחלה זהה למחלת הכבש הנגוע. כיוון שהגורם המדביק, בדומה לנגיפים, קטן דיו כדי לעבור דרך מעברים דקיקים של מסננים עדינים, נקראו מחלות אלה בשם "מחלות של נגיפים בלתי קונבנציונאליים". בשנות ה-50, בעוד מחקר מחלת הסקרפי מתנהל לאיטו, התחקתה קבוצת חוקרים בראשות הנירולוג האמריקני קרלטון גידוצ'ק (Gajducek) אחר מחלת הקורו - מחלת מוח קטלנית שהייתה נפוצה בקרב שבטים מסויימים בגיניאה החדשה. גידוצ'ק חקר את אופן הידבקותם של בני השבט פורה במחלה קטלנית זו. לבד משפע ממצאים אנתרופולוגיים מרתקים, התברר כי מדובר במחלת מוח מידבקת, המתפשטת בגלל קניבליזם פולחני, שבו אוכלים בני השבט את גופות מתיהם. נציין כי בשפת אנשי פורה, קורו פירושו פחד.
כשהגיעו הממצאים הפתולוגיים של מוחות חולי קורו לידיו של חוקר מחלת הסקרפי האנגלי האדלו (Hadlow), הוא הבחין בדמיון בין מוחות חולי הקורו לבין מוחם של כבשים נגועי סקרפי, והוא כתב על כך לגידוצ'ק. היום ידוע ששתי מחלות אלו נכללות בקבוצה גדולה יותר של מחלות מוח קטלניות - מחלות פריונים. בכולן רקמת המוח ספוגית. בקבוצה זו נכללות גם כמה מחלות תורשתיות של האדם: מחלת קרויצפלד-יעקב (CJD) וכן שתי מחלות עצבים נדירות יותר, GSS ו-FFI.

תמונה 1: ילידים מגיניאה החדשה מהאיזור ההררי שהיה נגוע בעבר במחלת הקורו
סקרפי במכרסמים
כל עוד הוגבל מחקר מחלת הסקרפי לכבשים בלבד, הוא התנהל באיטיות רבה, כיוון שהדגירה של המחלה בכבשים אורכת כשנתיים. בשנות ה-60 מצאו חוקרים סקוטים כי גם עכברים ואוגרים יכולים להידבק במחלה; בחיות קטנות אלו זמן הדגירה נמשך מספר חודשים. מאז הואץ קצב המחקר, והתברר באופן חד משמעי שהגורם האחראי למחלת הסקרפי אכן שונה מכל גורם שהיה ידוע קודם לכן. בעיקר התברר שגורם זה עמיד בפני חומרים וגורמים פיזיקליים הידועים כפוגעים בחומצות גרעין; לעומת זאת הוכח שכושר ההדבקה של גורם המחלה תלוי בחלבון (או חלבונים) לא מוכר. כאשר התגלה בשנת 1980, במעבדתו של סטנלי פרוסינר (Prusiner) מאוניברסיטת קליפורניה בסן-פרנסיסקו, החלבון המרכיב את גורם ההדבקה, נפתח העידן המודרני בחקר מחלות פריונים. פרוסינר זוכה בחודש זה בפרס וולף היוקרתי, כציון לתרומתו החשובה בחקר הפריונים. מהם פריונים?
בסוף שנות השבעים פותחו במעבדתו של פרוסינר שיטות לבידודו של הגורם המדביק ממוחות אוגרים נגועי סקרפי. שיאם של מאמצים אלה היה בידודו של תרחיף בעל כייל (ריכוז חומר) מדביק גבוה מאוד. לו היה גורם המחלה נגיף רגיל, הרי שמתרחיף מרוכז שלו היה אפשר להפיק, מלבד חלבונים, כמות גדולה של חומצות גרעין. החוקרים הוכו בתדהמה כשהתברר להם כי התרחיף הכיל מעט מאוד חומצות גרעין, ולעומת זאת חלבון אחד נמצא בו בכמות ניכרת. בבחינה במיקרוסקופ האלקטרונים לא נתגלו בתרחיף נגיפים, אלא "מקלות" (rods) זעירים. תגליות אלו עוררו את פרוסינר להציע - במאמר שפורסם בכתב-העת המדעי סאיינס (Science) ב-1982 את המושג פריון, שהוגדר אז כך: "חלקיק מעביר מחלה, התלוי בעיקרו במרכיבים חלבוניים". (המונח פריון נגזר מתיאורו: proteinacious infectious, כלומר: "מדביק חלבוני"). לחלבון שבפריון קרא פרוסינר PrPSc, דהיינו - צורת הסקרפי של חלבון הפריון. ההשערה שחלקיק מעביר-מחלה מורכב בעיקרו מחלבונים ואינו נושא עמו חומר גנטי בצורת חומצות גרעין התקבלה בעולם המדעי בספקנות ואפילו בעוינות. (כקוריוז היסטורי נזכיר, כי חוקר החלבונים החשוב בן המאה ה-19 רודולף וירכוב, ניסה להסביר הופעת מחלות זיהומיות בשינויים המתרחשים בחלבונים; הרעיון שחיידקים הם המעוררים מחלות זיהומיות לא הלהיב אותו). חלקיק כגון זה סתר לכאורה את ה"דוגמה המרכזית" של הביולוגיה המולקולרית, שלפיה חלבונים נוצרים על פי תבנית המוצפנת בחומצות גרעין.
נשאלה השאלה: היכן שוכן הגן, הכולל את המידע לבנייתו של חלבון הסקרפי? התשובה הייתה מפתיעה אפילו יותר ממה שציפו החוקרים: התברר שאת חלבון הסקרפי מקודד ה-DNA של תאי מוח החולה, ולא החלקיק המדביק! מצב זה שונה לגמרי מהמצב במחלה נגיפית, שהרי הנגיפים עצמם הם הנושאים את המידע לבניין חלבוניהם.
לאחר שיצרו החוקרים בסן-פרנסיסקו נוגדנים ייחודיים לחלבון הסקרפי של הפריון, התברר שנוגדנים אלו מזהים גם חלבון נוסף, הנמצא במוחם של אוגרים בריאים, שאינם חולים בסקרפי. חלבון זה נקרא בשם "החלבון התאי של הפריון" או בקיצור PrPc, והוא שונה בתכונותיו מחלבון הסקרפי של הפריון.
שני שחקנים מצויים עתה במגרש, הלא הם שתי התצורות של חלבון הפריון: התצורה התקינה, היא החלבון התאי של הפריון, שנקרא לה בקיצור "החלבון התקין", ותצורת הסקרפי הפגומה שנקרא לה "חלבון הסקרפי הפגום". מאז 1980 הצטברו ראיות לרוב, מכל תחומי הביולוגיה, שחלבון הסקרפי הפגום הוא אכן מרכיבו העיקרי, אם לא היחיד, של הפריון. תפקיד מרכזי בהוכחה היה לעכברים מהונדסים (עכברים טרנסגניים, ראו תמונה 2). נשאלה השאלה: מהו ההבדל בין שני החלבונים? במה שונה חלבון הסקרפי הפגוע המרכיב חלקיק מדביק, מהחלבון התאי התקין השוכן בקרומיות התאים של מוח בריא? ועלו גם תהיות: האם ייתכן שהחלבון התקין אכן מכפיל את עצמו במנגנון שאינו תלוי כלל בחומר הגנטי? שאלות אלו ניסרו בחלל עולם המדע, והחוקרים היטלטלו בין ספקנות לבין תדהמה. הנסיונות לפתור חידות אלו העסיקו את חוקרי הפריונים ברחבי העולם במשך כל העשור האחרון, ורק בשנים האחרונות מסתמנות תשובות משכנעות. התברר שלשני חלבוני הפריון אותו רצף של חומצות אמינו, שהן "אבני הבניין" המרכיבות את החלבונים (ראו תיבה). במה, אפוא, מתבטא ההבדל ביניהם? מתוצאות שהתקבלו לאחרונה, ועל פי ניתוח תאורטי של תוצאות ניסיוניות, משערים כיום ששתי תצורות החלבון נבדלות זו מזו בצורת ההתארגנות שלהן במרחב: החלבון התקין עשיר במבנים סליליים - סלילי אלפא (α-helices), ולעומת זאת בחלבון הפגום - חלבון הסקרפי, מרובים המבנים הפחוסים הנקראים משטחי ביתא (β-sheets).
מבנה חלבונים
חלבונים מורכבים משרשרות של אבני יסוד המכונות "חומצות אמינו". לכל חלבון רצף שונה, וייחודי, של חומצות אמינו. בתהליך יצירת החלבון, לאחר קישור חומצות האמינו לשרשרת, מצורפים מרכיבים נוספים, כגון סוכרים, שחיוניים לתפקוד החלבון. לעתים קרובות, נגרעות בשלב זה מן השרשרת חומצות אמינו. השרשרת הארוכה מתקפלת בסופו של התהליך בצורה יחודית לכל חלבון. הבדלים בין חלבונים קיימים בכל רמות הארגון. במקרה של חלבוני הפריון, חלבון הסקרפי הפגום שונה מהחלבון התקין באופן קיפול השרשרת. שכפול של "חלבון בלבד" - הכיצד?
גילויו של החלבון התקין סייע בפיענוח אופן "שכפולו" של הפריון. כדי להסביר את הגידול העצום במספר מולקולות חלבון הסקרפי בעת המחלה לא היה עוד צורך להציע מנגנונים מוזרים ביותר, לפיהם חלבון הסקרפי נוצר ללא תוכנית של חומר גנטי. עתה די היה להניח שבזמן המחלה ממירות כמה מולקולות של החלבון התקין, מבין אלה המצויות מכבר במוח, את המבנה המרחבי שלהן למבנה המאפיין את חלבון הסקרפי הפגום. ואכן, בניסויים שנעשו בתרביות תאים מודבקים בסקרפי, התברר שחלבון הסקרפי הפגום נוצר מלכתחילה כחלבון תקין, ורק כעבור שעות אחדות רוכשות מעט ממולקולות החלבון התקין את תכונותיהן של מולקולות חלבון הסקרפי. התגבשה הדעה כי במחלות פריונים מתרחש תהליך של הפיכת מולקולות תקינות לפגומות, וזאת בהשראתן של מולקולות פגומות קיימות (תמונה 3).
החלבון הפתולוגי "כופה" את מבנהו המרחבי על מולקולות תקינות, וכך "מגייס" אותן והופך אותן למולקולות חלבון הסקרפי הפגום. על פי מודל זה, החלבון הפגום מבוסס על גן של החולה, השוכן בכרומוזום שלו. מודל אלגנטי זה להסבר אופן התרבותם של פריונים מכונה מודל "החלבון בלבד", והוא ילווה אותנו בהמשך. אם המודל נכון, הרי שבעל-חיים שאין לו חלבון פריון תקין אמור להיות חסין מפני פריונים, בהיותו נקי מ"חומר הגלם" הדרוש ליצירת פריונים. האומנם בעל חיים כזה קיים במציאות? ובכן, חוקרים מקבוצתו של צ'רלס ויצמן (Weizmann) בציריך השתמשו בטכנולוגיה חדישה כדי לבטל את גן הפריון של עכברים. לחיות מהונדסות-גנטית אלה הזריקו פריוני סקרפי. והנה, לא זו בלבד שהחיות לא חלו, אלא שגם לא נוצרו בהן פריונים חדשים. תוצאה מדהימה זו, שפורסמה ב-1992, גרמה - אולי יותר מכל ממצא אחר - לקבלת מושג הפריון בקרב החוקרים.
אם כי המנגנון המדויק הפועל בהמרת החלבון מתצורתו התקינה לזו הפגומה אינו ברור עדיין דיו, בניסויים ששתי קבוצות בארצות הברית ערכו בשנה האחרונה מסתמנת האפשרות לשכפל במבחנה את חלבון הסקרפי. אם אמנם יצליחו החוקרים בכך, תהיה זו הוכחה כי פריונים מדביקים "התרבו" מחוץ לתא חי.
תמונה 2: בשנים האחרונות פותחו שיטות של הנדסה גנטית שבהם מוסיפים גנים לכרומוזומים של עכברים; עכברים מהונדסים כאלה מכונים "עכברים טרנסגניים". במקביל פותחו שיטות לסילוק גנים מסויימים מכרומוזומים של עכברים. החדרת הגן לעכבר נעשית בדרך של הזרקת DNA זר לביצית מופרית, וסילוק גנים נעשה בתרביות של תאים עובריים. שתי השיטות מסייעות רבות בחקר תיפקודם של גנים. בתמונה: עכברים טרנסגניים הנושאים מוטציה בגן הפריון, חולים ספונטנית במחלת פריונים. | ||||
בכרומוזומים של עכברים הוחדר הגן לחלבון הפריון, הנושא מוטציה (ירוק). |
בגיל 7 חודשים מפתחים העכברים הטרנסגנים מחלת פריונים ספונטנית. |
הזרקת תמצית מוח של עכברים טרנסגניים חולים לעכברים בריאים מחוללת בהם מחלת פריונים. | ||
 עכבר בריא עכבר חולה | ||||
פריונים - המופע התורשתי
כזכור, אחד המאפיינים המפתיעים ביותר של מחלות פריונים הוא שיש להן מספר מופעים: לצד המחלות המידבקות, כגון קורו, מופיעות גם מחלות פריונים תורשתיות, כגון מחלת קרויצפלד-יעקב. היום ידוע כי כל מחלות הפריונים התורשתיות קשורות לפגם גנטי - מוטציה בגן האחראי על ייצור החלבון התקין של חלקיק הפריון. כיום מוכרות כ-15 מוטציות בגן של החלבון, מוטציות הקשורות באופן מובהק למחלות פריונים משפחתיות-תורשתיות. זיהויין של מוטציות אלה פתח אפשרויות חדשות באבחון מחלות מוח ניווניות. האם המוטציות גורמות באופן ישיר למחלה? שאלה זו נבחנה בניסוייה של קרן שאו (Hsiao) במעבדתו של פרוסינר. החוקרת החדירה לעכברים גן לחלבון פריון תקין, ובו אחת המוטציות. התברר כי צאצאיהם של עכברים טרנסגניים אלה אכן חלו - ללא הזרקה של פריונים מבחוץ - במחלה דמוית פריונים ובגיל צעיר יחסית. יתר על כן, במוחם של עכברים אלה נמצאו פריונים שיכולים להדביק במחלת פריונים עכברים רגילים! תוצאה זו אוששה את ההנחה שמוטציות בגן האחראי על יצירת חלבון הפריון התקין הן הגורמות באופן ישיר להופעת מחלת פריונים אצל נשאי המוטציה (תמונה 2). כיצד גורמת מוטציה כזו להופעת המחלה? מודל ה"חלבון בלבד" מניח כי החלבונים המוטנטים נוטים מאליהם לקבל מבנה של חלבון פגום באמצעות שינוי שחל במבנה המרחבי שלהם. בעקבות זאת נוצר "זרע" או "תחל" פריוני, הגורם להתפשטות המחלה במוח החולה (בדומה ל"אפקט הדומינו" שתואר בתמונה 3) ולהופעת המחלה בגיל מבוגר.
תמונה 3: התפשטותו של חלבון הסקרפי של הפריון בתאי המוח קורה על-ידי תהליך הדומה ל"אפקט דומינו". התהליך מתחיל (א) כאשר מולקולה אחת של חלבון סקרפי (אדום) מתקשרת לחלבון פריון תקין (חום), וגורמת לו להתקפל למבנה המרחבי של חלבון הסקרפי (ב). בהמשך, חלקיקי הסקרפי מתקיפים מולקולות פריון תקינות נוספות (ג). מולקולות אלה הופכות לחלבוני סקרפי ואלה מתקשרים לחלבונים תקינים וחוזר חלילה, עד שחלקיקי הסקרפי מגיעים לרמות מסוכנות. | 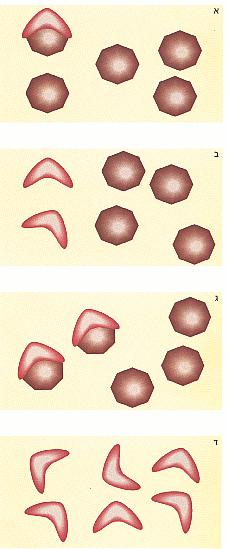 |
אולי בכל זאת נגיף?
אם כי מודל "החלבון בלבד" מסביר באופן פשוט ואלגנטי את רוב תכונותיהם של הפריונים, עדיין נשקלים במעבדות שונות מודלים אחרים לגבי מהותו של גורם המחלה. במיוחד נשקלת האפשרות שבפריון מצויות, מלבד מולקולות חלבון פגומות, גם מולקולות נוספות, שטרם זוהו. שמרניים ביותר הם תומכי הרעיון שמחולל מחלת הסקרפי הוא נגיף, אם כי נגיף לא קונבנציונלי. לטענת חוקרים אלה, הכשל בגילוי חומר תורשתי בפריונים עד כה איננו אלא כשל טכני. עם זאת, בשנים האחרונות אימצו רוב חוקרי הפריונים מושגים הקרובים למודל הפשוט של "חלבון בלבד". הפריונים והפרה המשוגעת
בתחילת שנות ה-80 החלו פרות לחלות במקומות שונים באנגליה, במחלת עצבים מסתורית. המחלה התפשטה לממדי מגפה, שבשיאה הושמדו כ-1000 פרות נגועות בכל שבוע. עבודה מאומצת של רשויות הבריאות הביאה, ב-1986, לתגלית מדהימה - לראשונה בהיסטוריה חלו פרות במחלת פריונים. בפרות אלה נתגלו כל סימני מחלות הפריונים, כגון תמונת המוח הספוגי, וכן חלבון הסקרפי הפגוע. המחלה מכונה BSE והחלבון הפתולוגי מכונה לפיכך PrPBSE כלומר - חלקיק הפריון של BSE. ההכרה בקיום מחלת פריונים בפרות השרתה דאגה עמוקה בקרב רשויות הבריאות ובקרב צרכני הבשר ומוצריו. התעורר חשש שמא מחלת הפרות עלולה לעבור לבני אדם ולגרום למגפה נרחבת של מחלת קרויצפלד-יעקב בבריטניה.
הופעתה הפתאומית של מחלת הפרות, ובהיקף כה גדול ברחבי בריטניה, נובע כנראה ממקורות המזון של הבקר בעדרים הנגועים. להעשרת תזונתן של הפרות הוסיפו למזונן חלבונים מן החי, המופקים מחלקי בעלי חיים שאין אפשרות לשווקם לצרכים אחרים. הסברה היא שתוספות אלו מורכבות גם מבשר של כבשים הנגועות בסקרפי, שהיא מחלה מאותרת (אנדמית) בבריטניה. והנה, התברר כי בסוף שנות השבעים החלו לעבד את מזון הפרות בטמפרטורות נמוכות יותר, ושינוי זה אפשר כנראה לפריונים של כבשים להדביק, לראשונה בהיסטוריה, אלפי פרות ברחבי הממלכה המאוחדת. לכאורה, מוח הפרה, כמו גם מוח הקניבל, מוגן היטב בקו הגנה כפול, מפני חלבונים מזיקים שבמזון. ראשית, חלבונים אינם עוברים בדרך-כלל מחלל המעי אל הדם, כי אם מתפרקים לחומצות אמינו. שנית, בין הדם לרקמת המוח קיים מחסום (המחסום הדמי-מוחי) המונע מעבר של חומרים רבים, בהם כאלה שהמולקולות שלהם קטנות בהרבה ממולקולות חלבון. ואמנם, נראה שחדירת חלבוני הפריון לגוף נעשית דרך פצעים זעירים שברירית הפה, והכניסה למוח עצמו נעשית דרך סיבי עצבים, ולא באמצעות זרם הדם. מבחינה זו יש בכך דמיון-מה למחלות מוח נגיפיות כמו כלבת.
אחד ממאפייני מחלות פריונים הוא המחסום בין המינים הביולוגיים (species), המתבטא בכך שפריונים המופקים מבעל חיים מסוים מדביקים בקלות את בני מינו הביולוגי, ולעומת זאת הידבקותם של בעלי חיים מסוג אחר נעשית אך בקושי.
מהו הסיכוי שמחלת הפרות תועבר לבני אדם? בשאלה זו קשור, כמובן, המחסום שבין המינים-הביולוגיים, ובמקרה זה - בין פרה לאדם. מחסום זה נובע, ככל הנראה, מההבדל שברצף חומצות האמינו של חלבוני חלקיקי הפריונים בשני המינים האלה. קשה מאוד לשער את מידת הסיכון הקיימת, מפני שהמנגנונים האחראים לקיומו של המחסום שבין המינים אינם ברורים עדיין כל צורכם. ייתכן שגם כאן יבואו לעזרתנו עכברים טרנסגניים: חוקרים בריטים מבית החולים סנט-מרי שבלונדון הזריקו לאחרונה פריון פרה לעכברים הנושאים את גן הפריון התקין של האדם, ומצאו שזמן דגירת המחלה בחיות המהונדסות לא נפל מזה של עכברים רגילים, ששימשו כקבוצת ביקורת. ממצאים אלה, שפורסמו אך לאחרונה בכתב-עת המדעי החשוב נייצ'ר (Nature), רומזים (הגם שאינם מוכיחים סופית) על כי פריוני בקר אינם מדביקים במיוחד בני אדם. בינתיים ייסדו שלטונות בריטניה מעבדת ביקורת, ואחד מתפקידיה הוא לעקוב אחר מקרי מחלת קרויצפלד-יעקב ברחבי האיים הבריטיים.
עמילואידים
במוחם של בעלי חיים ואנשים הנגועים במחלות פריונים מצטבר לעתים חלבון הסקרפי הפגום בכעין רבדים חוץ-תאיים (plaques). לרבדים אלה של חלבון הסקרפי תכונות פיזיקליות מיוחדות והם מתוארים כ"משקעים עמילואידיים". רבדים חלבוניים דומים יש גם ברקמות של חולים בכמה מחלות אחרות. לדוגמה, במחלת אלצהיימר מצטברים עמילואידים המורכבים משברי חלבון. העמילואידים יוצרים משקעים סדורים, דמויי סיבים מיקרוסקופיים, של חלבונים או חלקי חלבונים. כזכור, גם חלבון הסקרפי הפגום יוצר, בתנאים מתאימים, כעין "מקלות" בעלי מבנה אופייני ותכונות של עמילואיד. במבחנה, לעמילואידים תכונות כימיות אשר מזכירות באופן מפתיע את התנהגותם של פריונים.
מתברר, כי חלבונים וחלקי חלבונים שיש להם נטייה ליצור עמילואידים, ניחנים בתכונות המוכרות לנו מתהליכי גדילה של גבישים. למשל, עמילואידים יכולים לגדול ו"להתרבות" בתמיסה! בתמיסה המכילה חלבונים או שברי חלבונים מתאימים, נוצרים סיבים עמילואידיים, אלא שהתהליך איטי ביותר. אך כאשר מוסיפים לתמיסה זו סיבים מוכנים ("בוגרים"), הסיבים פועלים כ"זרעים" המאיצים מאוד היווצרות של סיבים נוספים. האם מנגנון פשוט כגון זה אחראי להתרבותם של פריונים? הדעות על כך עדיין חלוקות, וחוקרים אחדים סבורים כי הצטרפות חלבון הסקרפי הפגום לסיבים עמילואידיים היא תופעה משנית, שקודמת לה המרת התצורה המרחבית של החלבון. מעניין לציין, עם זאת, שברצף של החלקיק החלבוני של הפריון יש כמה אזורים מחוללי עמילואידים. כיום אין בידי הרפואה תרופות לטיפול במחלות פריונים. עם זאת, יש מספר קבוצות של חומרים אשר מאיטים את קצב יצירת חלקיק הסקרפי הפגום בתרביות תאים, וכן מאריכים את ומן הדגירה של המחלה בעכברים ובאוגרים. בין חומרים אלה מצויות תרכובות הקושרות עמילואידים. יש לקוות שחומרים אלה יהוו את הבסיס לפיתוח תרופות יעילות בעתיד.
פריונים בשמרים
על פי הנחת "החלבון בלבד", פריון הסקרפי "מתרבה" על-ידי כפיית מבנהו המרחבי הפגום על מולקולות חלבון תקינות במוחו של החולה. האם יתכן שקיימים חלבונים נוספים, מלבד חלבון הפריון, הניחנים בתכונות כגון אלה של יכולת להתפשט על-ידי כפיית פגם מבני?
ובכן, יתכן ומספר פגמים מטבוליים מסתוריים הנצפים בשמרים ימצאו את הסברם בהתנהגות דמויית פריונים. מדובר בפגמים, אשר מזה שנים היוו תעלומה לגנטיקאים בשל צורת הורשתם המוזרה. החוקר האמריקני ריד ויקנר (Wickner) הציג לאחרונה נימוקים משכנעים, הקושרים את אחד הפגמים הללו להתנהגות דמויית פריון. הפגם הידוע כ-URE-3 נובע, לטענת החוקר, מקיפול פגום באנזים של השמר הנקרא ure2p. נראה, שבדומה לפריון הסקרפי עשוי גם פגם זה להתפשט בקרב מולקולות האנזים הזה בתא השמר, ובכך להתבטא כפגם מטבולי.
מעניין לציין, שפגם מטבולי זה מורש עם חלוקת תא השמר, מפני שכל תא בת יורש מספיק מולקולות פגומות כדי שגם בו תמשיך להתפשט התקלה. קצה הקרחון
גוללנו כאן את סיפורם של הפריונים, העומדים בבסיס אחת התעלומות הרפואיות המענינות ביותר בזמננו. מושג הפריון, אשר נתקל בעוינות כה רבה לכשהוצע לפני יותר מעשור שנים, התקבל בסופו של דבר על דעת רוב המדענים (ואפילו נעשה בו כבר שימוש במדע הבדיוני; למשל בספרו החדש של מייקל קריצ'טון, "העולם האבוד" - סיפור ההמשך ל"פארק היורה").
נגיפים הם טפילים, המנצלים לצורכיהם מנגנונים של התא המודבק. מבחינה זו, פריונים הם טפילים מושלמים, שאפילו את מרכיבם העיקרי (ואולי - הבלעדי) הם נוטלים מהתא המותקף. הצגנו כאן דעה רווחת, שפריונים מתרבים בדרך של "כפיית" שינויים בקיפול המרחבי של חלבונים תקינים. האם יש סיבה להניח שמנגנון כגון זה יהיה מוגבל לחלבון הפריון? ובכן, רבים חשים היום שתהליכים דמויי פריונים יתגלו במערכות אחרות בביולוגיה וברפואה. שתי מערכות המבוססות אולי על מנגנון דמוי פריון נמצאו בשנה האחרונה בשמרים (ראו תיבה). נראה שבינתיים נתגלה רק קצה הקרחון, וייתכן מאוד שנכונו לנו הפתעות רבות בשדה הפריונים כבר בעתיד הקרוב.



