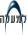כל התאים החיים, כולל תאי גופנו אנו, מכילים כמות גדולה של חלבונים. חלבוני התא מבצעים חלק ניכר מפעילויות התא - מהפקת אנרגיה ועד תנועה והפרשת חומרי פסולת. כדי שהחלבון ימלא את תפקידו בתא, הוא חייב להימצא במבנה התלת-ממדי המיוחד לו. אם בגופנו חלבונים רבים כל כך, מדוע אנחנו לא נהפכים ל"ביצה קשה" בכל כניסה לסאונה? מתברר כי באופן עקרוני הסכנה אכן אורבת, אך הגוף מתגונן בפניה בעזרת חלבונים מיוחדים הנקראים שפרונים (chaperones, מלשון: מלווים-שומרים). חלבונים אלה נמצאים בכל תא, והודות להם נמנעת ה"קטסטרופה". השפרונים הם חלבונים יציבים מאוד, שתפקידם להיצמד לחלבונים השרויים בסכנה של איבוד המבנה התקין שלהם ולהחזירם למצבם המתפקד. רוב השפרונים מנצלים אנרגיה של התא על מנת לבצע את פעילותם. בעשור האחרון חלה מהפכה בהבנת עולם השפרונים, וכיום ברור שבכל תא קיימים סוגי שפרונים רבים, הפועלים בצורות שונות ומגינים על התא הן במצבי עקה (לדוגמה, מכת חום או קור) והן בחיי היומיום.
חלבונים מלווים, מגינים, מעבירים ו"מיילדים"
לא רק בטמפרטורה גבוהה או בקור קיצוני שרויים החלבונים בסכנה של איבוד המבנה. כשחלבון נוצר בתא, הוא נוצר כשרשרת של חומצות אמינו (אבני הבניין של חלבונים) שאין לה המבנה התלת-ממדי המיוחד, ובזמן זה נמצא החלבון "הנולד" במצב רגיש מאוד ועלול להתקפל בצורה לא נכונה. הימצאות השפרונים ליד החלבונים ב"רגעי לידה" אלה מייצבת את החלבון במבנה הרצוי ומבטיחה שמרבית חלבוני התא יהיו מוכנים לפעולה. השפרונים גם עוזרים לשנע חלבונים ממקום למקום בתוך התא, ובעיקר - להעבירם לאברונים תוך-תאיים כגון המיטוכונדריונים (אברוני ייצור האנרגיה בתא) או הכלורופלסטים (אברוני הפוטוסינטזה בצמחים). תאים חיים משקיעים אנרגיה רבה בהגנת המבנה התקין של החלבונים שלהם. כאשר מערכות ההגנה נפגעות, חלבונים מתחילים לעבור שינוי צורה ויוצרים צברים. מצב כזה עלול להיות מסוכן מאוד לתא ואף לגרום למחלות קשות. כיום מקובל לחשוב שמחלות מוח ניווניות רבות, וביניהן אלצהיימר, נובעות מהופעת צברי חלבונים (אמילואידים) במוח, צברים הפוגעים בפעילות התקינה. גם מחלות הפריונים כגון מחלת "הפרה המשוגעת", נובעות מיצירת צברים של חלבוני הפריונים, כשהם מאורגנים במבנה תלת-ממדי שונה מהתקין (ראו: "חידת הפריונים", גליליאו 15, עמ' 17; "הפריונים המתעתעים", גליליאו 26 עמ' 65).
תמונה 1: למעלה: תהליכים תאיים הנעזרים בשפרונים. ניתן לראות כי שפרונים מגינים על החלבונים הנוצרים בריבוסומים (אתרי הייצור של החלבונים). שפרונים גם עוזרים בהעברת החלבונים לאברונים שונים המצויים בתא. כמו כן הם עוזרים לחלבונים פגומים להתקפל מחדש או לעבור פירוק. למטה: מבנה שפרונים שונים ואופן קשירתם לחלבון.
לשמור על האותות - ועל העובר
אחד השפרונים החשובים בתאים של בעלי חיים הוא החלבון HSP90 (ראשי תיבות של: Heat Shock Protein 90Kd). חלבון זה מהווה אחוז אחד מכלל החלבונים בתא; מאחר שבכל תא יש בסך-הכל אלפי חלבונים שונים, אחוז אחד פירושו אחוז ניכר ביותר! כמו לשפרונים רבים נוספים, גם לחלבון זה פעילויות הן בזמן "שלום" והן בעתות "חירום". כאשר התא נמצא במצב עקה חלבון זה חשוב בהגנה על כלל החלבונים התאיים מפני שינוי במבנה התלת-ממדי, שעלול אף לגרום ליצירת צברי חלבונים. במצבים אלה פועל HSP90 באופן לא סלקטיבי, על כל חלבון השרוי בצרה - הוא מזהה את החלבונים שאיבדו את המבנה התקין שלהם ובעזרת חלבונים נוספים עוזר להם לחזור לתפקד באורח תקין. בנוסף לפעילות זו יש לחלבון HSP90 תפקיד גם במהלך חיי התא התקינים. במצב רגיל, מזהה השפרון מספר מצומצם של חלבונים אליהם הוא נקשר באופן סלקטיבי. כיום ידועים יותר מ-20 חלבונים כאלה, אשר זקוקים לשפרון על מנת להגיע לקיפול נכון ולפעילות מלאה בתא. באופן מפתיע התברר שמרבית החלבונים הללו הם חלבונים הקשורים בתהליכי העברת אותות בתא, והם חשובים ביותר להתפתחות תקינה של העובר. בתהליך ההתפתחות העוברית נוצר יצור שלם המורכב מסוגי תאים רבים המסודרים באורח מופתי, וכל זאת מתא בודד, הביצית המופרית. התפתחות תקינה של עובר תלויה בכך שכל תא ותא "ידע" לבצע את הדבר הנכון בזמן הנכון. בכל שלב בהתפתחות יכול תא לבצע פעילויות שונות כגון: להתחלק, לנדוד,למות מוות תאי מתוכנן (אפופטוזיס; ראו: כרוניקה של מוות מתוכנן מראש", גליליאו 28) או להתמיין לתאים מסוגים שונים כגון: תא שריר או תא כבד. אם כל התאים פועלים כראוי אזי ההתפתחות העוברית היא תקינה. פעילות התא בכל רגע נתון נקבעת על ידי מגוון אותות, חיצוניים לתא ופנימיים בו. האותות מזוהים על ידי מגוון רחב של חלבונים (דוגמת קולטנים) המשנים את פעילותם בתלות במסר המתקבל. יש מקרים חריגים בהם תא אינו פועל לפי הוראות סביבתו, וכמעט תמיד הם מסוכנים. דוגמה לכך הם תאים סרטניים, שממשיכים להתחלק ללא קשר לאותות המורים להם להפסיק בכך. ברור, אם כן, מדוע חיוני שהמולקולות האחראיות על זיהוי האותות ועיבודם יהיו במצב הכן. וזה בדיוק תפקידו של HSP90 - הוא נקשר לחלבונים מזהי-אותות ושומר על המבנה התקין שלהם, מבנה המאפשר להם קישור למולקולות מאותתות.
למרות שהשפרון HSP90 כה נפוץ וכנראה כה חיוני לתא, לא הרבה ידוע על דרך פעילותו. החוקרות סוזן רתרפורד וסוזן לינדקוויסט (Rutherford, Lindquist) מאוניברסיטת קליפורניה ביקשו לפענח את תפקודו של HSP90 בדרך של ביטול פעילותו בתאים. הרעיון הוא שפגמים המופיעים בעקבות איבוד פעילותו של חלבון מסוים יכולים ללמד אותנו על פעילותו התקינה של החלבון. מכיוון שכל החלבונים מיוצרים על סמך המידע הנמצא בגנים, ומכיוון שבכל תא קיימים כרגיל שני עותקים של כל גן (אחד אבהי ואחד אמהי) יש צורך לבטל את שניהם כדי למנוע כליל את יצירת החלבון. ביטול ביטויו של חלבון על ידי מחיקת הגנים שמקודדים אותו נקרא "נוק-אאוט". החוקרות החליטו לבצע נוק-אאוט בזבובון התסיסה דרוזופילה. במאמר שפרסמו (נייצ'ר, 26 בנובמבר 1998), דיווחו כי כאשר ביטלו כליל את ביטויו של HSP90, הזבוב כלל אינו מתפתח. מת בשלב העוברי. פירוש הדבר הוא שמדובר בחלבון חיוני להתפתחות תקינה של הזבוב. ואולם בשיטה זו לא מתאפשרת בחינה מדוקדקת יותר של השפעת החלבון. לפיכך בדקו זבובים שבהם נשמר עותק אחד של הגן (זבובים הטרוזיגוטים). בתחילה נראה היה שאין שום השפעה להפחתת כמות HSP90 - מכיוון שהזבובים בקעו והתפתחו באופן תקין. ואולם כאשר בחנו מספר רב מאוד של זבובים התברר שאחוז לא מבוטל מן הזבובים לוקים בפגמים. עובדה מפתיעה במיוחד שנתבררה היא שהזבובים הפגומים (מוטנטים) נבדלים זה מזה באופי הפגיעה: לחלק יש כנף קטנה מהרגיל, לחלק מחושים מנוונים, לחלק מהם עיניים מעוותות. מדוע זה מפתיע? מפני שכרגיל פגיעה בפעילותו של חלבון מסוים גורמת להיווצרות אותם פגמים בכל הפרטים בעלי החלבון הפגום. לדוגמה: פגיעה בגן האחראי על התפתחות העין תגרום תמיד לפגם בעיניים. נדיר לראות מצב שבו אותה פגיעה עצמה בפרטים שונים גורמת לפגמים מסוגים לגמרי שונים.
תמונה 2: מראה של זבובים הפגועים בשפרון HSP90. |
 |
לסתור פגמים נסתרים
החוקרות העלו השערה לפיה ההופעה השונה מפרט פגוע אחד למשנהו נובעת מכך שהפגיעה בחלבון גורמת באופן כלשהו לעליה בתדירות הופעת המוטציות עליה בתדירות המוטציות גורמת לפגמים אקראיים בגנים שונים, וכתוצאה מכך להופעת שינויים מגוונים במראה בעלי-החיים ובתפקודם. מצבים כאלה מוכרים גם באדם: יש מחלות הנגרמות כתוצאה מפגיעה בחלבונים המתקנים פגמים בדנ"א. ללא חלבוני תיקון אלה מצטברות מוטציות; הדבר מתבטא בבעיות רפואיות רבות, וביניהן תדירות גבוהה של גידולים סרטניים.
כדי לבדוק את ההשערה הכליאו החוקרות את הזבובים נושאי המוטציה עם זני זבובים שאינם נושאים את המוטציה ושמקורם במקומות שונים בעולם. בהכלאה כזו מחצית הצאצאים מקבלים גן אחד פגום, וצאצאים אלה ניתן לבדוק. למרבה ההפתעה התברר שבצאצאי ההכלאות עם הזנים השונים התגלו מוטציות שונות; בכל זן נתגלו מוטציות אופייניות לו. נראה, אם כן, שלא מדובר בקצב מוגבר של יצירת מוטציות חדשות - שהרי אז היו הפגמים מפוזרים אקראית - אלא שהפגיעה בחלבון HSP90 רק חושפת "אל פני השטח" (כלומר - מעוררת התבטאות) מוטציות שהיו כבר קיימות מראש. ידועות כיום דרכים נוספות שבעזרתן ניתן להוריד את יעילות הביטוי של HSP90 בתאים. אחת הדרכים היא שימוש במעכב ספציפי (גלדנומיצין) שפוגע ביכולת החלבון לנצל אנרגיה תאית לצורך פעילותו. דרך נוספת היא ניצול תפקידו של החלבון עצמו בזמן עקת חום. כזכור, במצב כזה מטפל השפרון בכל החלבונים הפגומים בתא, ואז הוא פחות פנוי, כמובן, וזה מדמה מצב שבו יש פחות שפרון בתא. ואכן, הן כאשר האכילו רימות זבובים בגלדנומיצין והן כאשר חשפו אותן לטמפרטורות גבוהות, נתגלו בהן פגמים דומים לאלה שבניסוי המקורי. נראה, אם כן, כי הפגיעה בחלבון HSP90 היא אכן האחראית על מצב הזבובים. ועדיין נותרה פתוחה השאלה: איך ייתכן שחלבון אחד גורם לתופעה שונה בכל זבוב?
החוקרות הסיקו כי באוכלוסיות שונות של זבובוני תסיסה קיימים פגמים (מוטציות) במספר גנים שהחלבונים שהם מקודדים זקוקים ל- HSP90לצורך קיפולם התקין. המוטציות גורמות לכך שהחלבונים נעשים פגיעים יותר ונוטים לאבד בקלות את המבנה התלת-ממדי שלהם. במצב הרגיל השפרון מייצב חלבונים פגומים אלה במצבם התקין. כך שבאוכלוסיית זבובוני תסיסה רגילה אין צאצאים פגומים רבים; מדובר, אם כן, בכעין מוטציות נסתרות. לעומת זאת, כאשר קיים מחסור בשפרון, המוטציות הנסתרות הללו באות לידי ביטוי בחלבונים ומכאן - בפגמים בהתפתחות. פגיעה בפעילות של חלבון האחראי על זיהוי אות הגדילה של הכנף, למשל, תגרום להיווצרות כנף קטנה מדי או מעוותת. כלומר, החלבון HSP90 מסייע ב"מיסוך" של מוטציות הנמצאות בזבובים באופן טבעי, ומאפשר לחלבונים מוטנטים לתפקד באופן תקין.
קפיצת מדרגה בתיאוריית הקפיצות?
ההסבר המקובל כיום להיווצרות שפע המינים-הביולוגיים הוא זה של תיאוריית האבולוציה כפי שנהגתה על ידי דרווין והחוקרים ממשיכי דרכו. על פי תיאוריית האבולוציה המקורית, מהלך היווצרות המינים-הביולוגיים מבוסס על שינויים הדרגתיים שמקורם מוטציות. מוטציות אלו יכולות לפגוע בתפקוד הפרט הנושא אותן, אך גם להקנות לו יתרון הישרדותי כלשהו. מוטציה שמקנה לפרט יתרון רבייתי הופכת נפוצה באוכלוסייה, עד שבשלב כלשהו ייתכן שכל הפרטים באוכלוסייה ישאו מוטציה זו. גישה זו מסוגלת להסביר תופעות רבות בהשתנות של מינים-ביולוגיים, אך יש גם שאלות שעליהן קשה לענות בעזרתה. אחת הבעיות הקשות היא היווצרות של קבוצות גדולות חדשות (משפחות, מחלקות, ממלכות), מכיוון שבמהלך היווצרותן מתרחשים לעתים שינויים עמוקים רבים בה-בעת, ולא בצורה הדרגתית והמשכית. מקרה נוסף שבו נדרשים שינויים רבים המתרחשים בה-בעת הוא שינוי של מערכות מורכבות ביצורים חיים, כמו מערכות של העברת אותות תאיים. במערכת כזאת, בדרך כלל שינוי של רכיב יחיד במערכת יגרום לקריסתה, אך שינוי מקביל בכל רכיביה של מערכת יכול להפוך אותה ליעילה יותר או להקנות לה פעילויות נוספות. על כן גם שינויים במערכות של הובלת אותות תאיים קשה להסביר על ידי אבולוציה הדרגתית. אחת התיאוריות שהוצעו בשנים האחרונות בניסיון להתמודד עם הקשיים הללו היא תיאוריית האבולוציה בקפיצות שנוסחה על ידי חוקר האבולוציה והסופר הידוע סטיבן גולד ועמיתו ניילס אלדרידג' (Gould, Eldredge). בעוד שדרווין טען שמרבית השינויים במהלך האבולוציה התרחשו באופן הדרגתי ומתמשך, טענו גולד ואלדרידג' כבר ב-1972 שמרבית השינויים מתרחשים בקפיצות פתאומיות, שביניהן זמנים ארוכים של יציבות וקביעות, תקופות בהן המערכת נמצאת בשיווי משקל. מחקר המאובנים ניתן ללמוד על תקופות של יציבות עולמית, שהצטיינו ברציפות סוגי המינים המאובנים, ובצידן מעברים פתאומיים מתקופה אחת לאחרת. עד היום כמעט שלא נמצאו דוגמאות לשינויים הדרגתיים במין-ביולוגי מסוים, אלא מקרים של שינויים מבניים גדולים. תומכי האבולוציה ההדרגתית נהגו לטעון שאוסף המאובנים אינו מושלם, ולכן איננו רואים את צורות הביניים. ואולם עם ההרחבה הניכרת באוספי המאובנים במהלך השנים האחרונות מתברר שאכן נדיר למצוא צורות ביניים, וכנראה שהשינויים האבולוציוניים הגדולים אכן מתרחשים בקפיצות. למרות שתיאוריית האבולוציה בקפיצות כבר מקובלת למדי, לא היו מובנים המנגנונים הגנטיים שיכולים להסביר אבולוציה שאיננה הדרגתית.
אחד ההסברים הפשוטים לתופעה הוא שינויים ברמה של כרומוסומים שלמים - תוספת של כרומוסום או מספר כרומוסומים. מאחר שכל כרומוסום נושא אלפי גנים, שינוי כזה הוא פעמים רבות קטלני, אך במקרים נדירים יכול לגרום גם לקפיצה התפתחותית משמעותית. והנה, רתרפורד ולינדקוויסט טוענות שייתכן כי בידיהן הסבר מולקולרי ראשון לאבולוציה בקפיצות - השפרון HSP90. הן מציעות כי הוא ממסך מוטציות המצטברות והולכות באופן סמוי במהלך התקופות היציבות, ואז, במצבי עקה, כאשר רמת תפקודו של השפרון יורדת, מתגלים בבת-אחת שינויים גדולים ונעשות הקפיצות ההתפתחותיות. מצבי העקה בהם מדובר הם, למשל, התחממות גלובלית או תקופות קרח. סביר להניח שמרבית הפרטים באוכלוסייה נפגעים קשות מן השינויים הרבים שמופיעים בהם. אך בתוך אוכלוסיות ענקיות ייתכן שבפרטים בודדים השינוי הגדול יביא לשיפור בהישרדות, כך שתהיה סלקציה לטובתם. לאחר מספר דורות הם יהוו את רוב האוכלוסייה ונהיה עדים ל"קפיצה" בתכונות, ואולי אף להופעת מין-ביולוגי חדש.
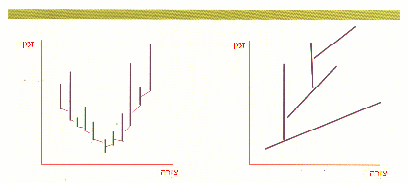
תמונה 3:
מהלך התפתחות המינים על פי שתי תיאוריות של האבולוציה: התיאוריה ההדרגתית ותיאוריית הקפיצות.
מימין: התיאוריה ההדרגתית. שינוי איטי ומתמיד בצורה לאורך הזמן.
משמאל: תיאוריית הקפיצות. תקופות ארוכות יחסית ללא שינוי צורה וביניהן קפיצות.
שיפורים לתיאוריית השפרונים
התיאוריה של החוקרות מקליפורניה מתייחסת לחלבון HSP90 אותו חקרו. אמנם, שפרון זה פועל על מספר עשרות חלבונים תאיים, ובכל זאת מדובר באחוז קטן מכלל חלבוני התא. בשל עובדה זאת, פגיעה ב- HSP90יכולה לגרום לשינויים במספר מוגבל של תכונות. כדי לבסס את תהליכי הקפיצות באבולוציה על עיקרון מעין זה, חייבים להיות שפרונים נוספים שישמשו כ"ממסכי מוטציות" או חלבונים אחרים שיפעלו בצורה דומה. מחקרן של רתרפורד ולינדקוויסט עורר הדים בקרב חוקרי האבולוציה, וודאי יהווה נקודת מוצא לחיפוש אחר גנים נוספים המסוגלים לתפקד בצורה דומה. לא רק חוקרי האבולוציה הושפעו מן התוצאות, אלא גם הגנטיקאים, ובעיקר גנטיקאים של האדם. כיצד משפיע מחקר בהתפתחות של זבוב התסיסה דרוזופילה על חקר הגנטיקה של האדם? המחקר של מחלות גנטיות באדם מתמקד במציאת הגנים הפגועים במחלות שונות, ובאיתור השינויים ברצף הנוקליאוטידים (אבני-הבניין של הדנ"א) בגנים הפגומים. מן המחקר בזבוב התסיסה מתברר שגם מוטציות שנראות לכאורה "לא מזיקות" יכולות, בתנאים מסוימים, להשפיע בצורה קיצונית על תפקוד החלבון. ייתכן שחולה אחד לוקה במחלה באופן קשה יותר מחולה אחר בגלל אותם שינויים שמרניים הקיימים אצלו והמשפיעים רק תחת מצבים מסוימים בתא. ייתכן שיש בכך משום פתח לחשיבה מחודשת בתחום הגנטיקה של האדם.